免疫组化
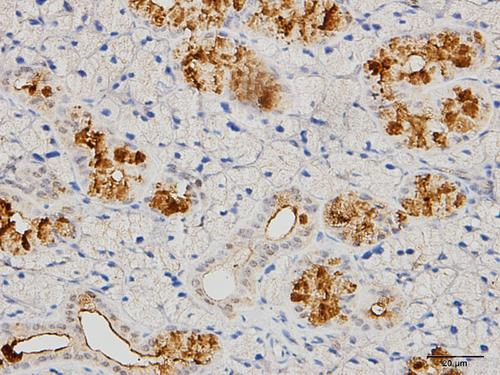
免疫组化(Immunohistochemistry,IHC)是利用抗原抗体反应,即抗原与抗体特异性结合的原理,通过化学反应使标记抗体的显色剂(荧光素、酶、金属离子、同位素)显色来确定组织细胞内抗原(多肽和蛋白质),对其进行定位、定性及定量的研究。
众所周知,抗体与抗原之间的结合具有高度的特异性。免疫组化正是利用这一特性,即先将组织或细胞中的某些化学物质提取出来,以其作为抗原或半抗原去免疫小鼠等实验动物,制备特异性抗体,再用这种抗体(第一抗体)作为抗原去免疫动物制备第二抗体,并用某种酶(常用辣根过氧化物酶)或生物素等处理后再与前述抗原成分结合,将抗原放大,由于抗体与抗原结合后形成的免疫复合物是无色的,因此,还必须借助于组织化学方法将抗原抗体反应部位显示出来(常用显色剂 DAB显示为棕黄色颗粒)。通过抗原抗体反应及呈色反应,显示细胞或组织中的化学成分,在显微镜下可清晰看见细胞内发生的抗原抗体反应产物,从而能够在细胞或组织原位确定某些化学成分的分布、含量。组织或细胞中凡是能作抗原或半抗原的物质,如蛋白质、多肽、氨基酸、多糖、磷脂、受体、酶、激素、核酸及病原体等都可用相应的特异性抗体进行检测。
免疫组化实验所用标本主要有组织标本和细胞标本两大类,前者包括石蜡切片(病理切片和组织芯片)和冰冻切片,后者包括组织印片、细胞爬片和细胞涂片。其中石蜡切片是制作组织标本最常用、最基本的方法,对于组织形态保存好,且能作连续切片,有利于各种染色对照观察;还能长期存档,供回顾性研究;石蜡切片制作过程对组织内抗原暴露有一定的影响,但可进行抗原修复,是免疫组化中首选的组织标本制作方法。
免疫组化实验中常用的抗体为单克隆抗体和多克隆抗体,单克隆抗体是一个B淋巴细胞克隆分泌的抗体,应用细胞融合杂交瘤技术免疫动物制备。多克隆抗体是将纯化后的抗原直接免疫动物后,从动物血中所获得的免疫血清,是多个B淋巴细胞克隆所产生的抗体混合物。
免疫组化是一个既简单又复杂的实验技术:原理很简单,但是结果受很多因素如固定时间、固定剂的选择、抗原修复方法等影响。所以,要想得到高质量的结果,应从取材固定开始避免引入误差。